La recherche médicale & la NF1
Durant de nombreuses années, la neurofibromatose était relayée sur le côté concernant les recherches médicales. Pas assez porteuse financièrement. Les chercheurs préféraient baser leurs investissements sur des maladies plus répandues.
Heureusement, ce n’est plus le cas à l’heure actuelle.
En voici la preuve !
À ce jour, 245 études trouvées concernant la Neurofibromatose À travers le monde.
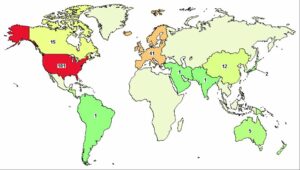
En 2021, en date du 7 avril, 211 études sont encore actives.
Nous allons aborder 4 recherches intéressantes dont nous avons accès aux résultats. Comme vous pourrez le remarquer, il n’est malheureusement pas évident lorsque l’on entame une recherche d’aboutir aux résultats escomptés.
Nous vous souhaitons une bonne lecture !
- Évérolimus pour le traitement des lésions cutanées défigurantes en neurofibromatose 1 CRAD001CUS232T (DCLNF1)
Parrainée par le Centre des sciences de la santé de l’Université du Texas, Houston avec la collaboration avec la Fondation Texas Neurofibromatosis
La sécurité et la validité scientifique de cette étude relèvent de la responsabilité du promoteur de l’étude et des investigateurs. La liste d’une étude ne signifie pas qu’elle a été évaluée par le gouvernement fédéral américain
Tous les participants (24) à l’étude recevront Everolimus à une dose initiale de 10 mg par jour et seront ajustés à la hausse ou à la baisse de 2,5 mg à intervalles de 2 semaines pour atteindre une concentration minimale de 5 à 15 ng / mL. 7 participants ont abandonnés l’étude.
Effets indésirables. (Nous avons repris les % les plus élevés)

- Neurobiologie et traitement des troubles de la lecture dans la NF-1
Parrainée par l’université Vanderbilt avec la collaboration de l’institut national des troubles neurologiques et des accidents vasculaires cérébraux (NINDS)
La sécurité et la validité scientifique de cette étude relèvent de la responsabilité du promoteur de l’étude et des investigateurs. La liste d’une étude ne signifie pas qu’elle a été évaluée par le gouvernement fédéral américain
Bref résumé :
- Le but de cet essai est de déterminer si les enfants atteints de neurofibromatose de type 1 qui ont des troubles de lecture répondent de la même manière – à la fois comportementale et neurobiologique – aux programmes de traitement spécialisés que les enfants ayant des troubles de lecture idiopathiques, et de déterminer quelle intervention convient le mieux à un apprenant particulier profils.
Description détaillée:
- La préoccupation la plus courante des parents d’enfants atteints de neurofibromatose de type 1 (NF-1) concerne les troubles d’apprentissage (TA). Environ la moitié de tous les enfants atteints de NF-1 ont des TA, dont les plus débilitants et les plus courants sont des troubles de la lecture.
- Le but de cette étude est de déterminer si les enfants atteints de NF-1 qui ont des troubles de lecture répondent de la même manière – à la fois comportementale et neurobiologique – aux programmes de traitement spécialisés connus pour améliorer les déficits de décodage chez les enfants ayant des troubles de lecture idiopathiques. L’essai déterminera également quelle intervention convient le mieux à certains profils d’apprenants. Le but général de cette recherche est d’acquérir une compréhension plus approfondie des caractéristiques et du traitement des troubles de la lecture dans la NF-1.
- Dans l’essai, les chercheurs compareront des enfants atteints de NF-1 qui présentent des faiblesses en lecture à des enfants ayant des troubles de lecture sans cause connue (idiopathique) en utilisant deux interventions différentes et des mesures comportementales et neurobiologiques. Les deux interventions se concentrent sur l’enseignement des relations son-symbole, mais varient en termes d’emphase relative sur les méthodes d’enseignement verbales et visuelles.
- Les scientifiques espèrent que les résultats de l’essai feront progresser les connaissances sur les meilleures thérapies pour la DL chez les enfants atteints de NF-1. Et, en affinant davantage la façon dont les enfants atteints de NF-1 qui ont des troubles de lecture sont similaires (ou différents) aux enfants ayant des troubles de lecture idiopathiques, les chercheurs pourraient être en mesure de savoir si les interventions de lecture qui abordent des domaines autres que le décodage bénéficieront également aux enfants atteints de NF. -1. De plus, en comprenant les similitudes et / ou les différences dans les profils neuropsychologiques et neurobiologiques des enfants atteints de NF-1 qui ont des troubles de lecture et de ceux qui n’en ont pas, les scientifiques pourront affiner le phénotype cognitif et les caractéristiques neurobiologiques de NF-1, ce qui une meilleure compréhension des anomalies du système nerveux central dans la NF-1.
Vous pouvez retrouver les résultats de cette étude via une vidéo sur le site : https://ebrl.vkcsites.org/
- Étude de Tasigna®/Nilotinib (AMN107) chez les patients atteints de neurofibromatoses (NF1) atteints de neurofibromes plexiformes
Identifiant ClinicalTrials.gov: NCT01275586, parrainé par l’ Université de l’Indiana en collaboration avec Novartis
La sécurité et la validité scientifique de cette étude relèvent de la responsabilité du promoteur de l’étude et des investigateurs. La liste d’une étude ne signifie pas qu’elle a été évaluée par le gouvernement fédéral américain.
Après l’inscription, chaque sujet recevra initialement Tasigna par voie orale à raison de 200mg deux fois par jour pendant deux semaines. Si ele est tolérée, la dose sera augmentée à 300mg deux fois par jour après un minimum de deux semaines et sera augmentée à une dose de 400mg deux fois par jour après deux semaines supplémentaires si elle est tolérée.
6 participants et trois ont abandonné en cours d’étude.
Résultat principal


- Étude du PEG-Intron pour les neurofibromes plexiformes
Parrainé par l’ Université de Pittsburgh en collaboration avec l’Institut national du cancer (NCI)
La sécurité et la validité scientifique de cette étude relèvent de la responsabilité du promoteur de l’étude et des investigateurs. La liste d’une étude ne signifie pas qu’elle a été évaluée par le gouvernement fédéral américain
Description de l’étude
Bref résumé:
Cette étude concerne les tumeurs à croissance lente appelées neurofibromes plexiformes (PNF) qui sont un problème relativement courant chez les personnes atteintes de neurofibromatose de type 1 (NF1). Ces tumeurs sont bénignes, mais à mesure qu’elles se développent, elles peuvent devenir défigurantes, invalidantes ou même mortelles. Ils provoquent souvent des douleurs, des difficultés à utiliser les bras ou les jambes en raison de la compression de la moelle épinière et / ou des lésions nerveuses. À l’heure actuelle, la seule thérapie disponible pour les neurofibromes plexiformes est d’essayer d’enlever chirurgicalement autant de tumeur que possible. Parce que ces tumeurs se développent dans les zones environnantes, une résection chirurgicale totale est souvent impossible. La plupart des tumeurs repousseront après la chirurgie si la totalité de la tumeur ne peut pas être retirée. À ce jour, d’autres traitements, notamment la chimiothérapie et la radiothérapie, n’ont pas permis de réduire ces tumeurs.
- L’interféron est un médicament utilisé pour différents types de tumeurs ainsi que pour l’hépatite. Il a été utilisé dans le traitement des neurofibromes plexiformes (PNF) chez certains sujets présentant une amélioration des symptômes et / ou une diminution de la taille de la tumeur. La plupart des sujets n’ont pas eu de croissance supplémentaire de leur tumeur pendant le PEG-Intron. Le médicament utilisé dans cette étude est le PEG (pégylé) -Intron. Le PEG-Intron est une forme d’interféron à action prolongée qui empêche le médicament de se décomposer dans l’organisme pendant une période plus longue et pourrait potentiellement être plus efficace que l’interféron à action brève. PEG-Intron a été approuvé par la Food and Drug Administration (FDA) pour le traitement de l’hépatite C.
Les objectifs de cette étude sont:
- Déterminer comment le neurofibrome plexiforme de votre enfant répond au PEG-Intron lorsqu’il est administré chaque semaine.
- Déterminer les effets secondaires du PEG-Intron administré chaque semaine à des participants atteints de neurofibromes plexiformes.
- Évaluer une nouvelle méthode de mesure des changements de taille des tumeurs appelée analyse de volume. Cette méthode mesure le volume entier d’une tumeur en trois dimensions. La méthode standard de mesure des tumeurs utilise uniquement la longueur et / ou la largeur de la tumeur. En étudiant les différentes méthodes de mesure des tumeurs, les chercheurs espèrent pouvoir déterminer quelle méthode est la plus précise et la plus utile.
- Description détaillée:
- PEG-Intron sera administré chaque semaine au moyen d’une petite aiguille sous la peau, de la même manière que l’insuline est administrée aux personnes atteintes de diabète. Les sujets apprendront à le faire à la maison. Tant que la tumeur ne se développe pas et que les effets secondaires sont tolérables, les injections seront administrées une fois par semaine pendant 2 ans.
- Les enfants seront inscrits à l’étude dans l’une des trois strates (groupes de patients): la strate 1 comprend les enfants qui ne présentent aucun symptôme associé à leur PNF et les examens IRM au cours de l’année écoulée peuvent ou non montrer une croissance tumorale, la strate 2 comprend les enfants qui présentent des symptômes associés au PNF mais que les IRM au cours de l’année écoulée n’ont pas montré de croissance et la strate 3 comprend les enfants qui ont montré une augmentation de la taille du PNF sur les IRM au cours de l’année écoulée, avec ou sans symptômes.
Mesures des résultats
Mesures des résultats primaires :
Nombre de participants avec une réponse d’imagerie dans les strates 1 et 2
[Délai: des IRM ont été effectuées au départ et aux mois 4, 8, 12, 18 et 24 pendant le traitement et tous les 6 mois par la suite jusqu’à la fin de l’étude. ]Une réponse a été définie comme une réduction ≥ 20% de la somme du volume du neurofibrome plexiforme (NP) «cible» dans les 12 mois confirmée par une IRM de suivi après ≥ 4 semaines.
Réponse clinique dans la strate 2
[Période: ligne de base, semaine 6, mois 4, 8, 12, 18 et 24 pendant le traitement et tous les 6 mois par la suite jusqu’à la fin de l’étude]La réponse clinique a été définie comme une amélioration spécifiée dans le protocole de l’évaluation ophtalmologique, une amélioration d’au moins un niveau de l’indice de performance (PS) ≥ 50% de diminution de la quantité de médicaments contre la douleur requise par semaine par rapport à la valeur initiale ou de la capacité à passer d’un narcotique. à un analgésique non narcotique, maintenu pendant au moins un mois.
Temps de progression (TTP) dans la strate 3
[Période: ligne de base, semaine 6, mois 4, 8, 12, 18 et 24 pendant le traitement et tous les 6 mois par la suite jusqu’à la fin de l’étude]Le TTP a été estimé par la méthode Kaplan-Meter
Mesures des résultats secondaires :
Nombre de participants avec réponse d’imagerie dans la strate 3 [Période: des IRM ont été effectuées au départ et aux mois 4, 8, 12, 18 et 24 pendant le traitement et tous les 6 mois par la suite jusqu’à la fin de l’étude]Une réponse a été définie comme une réduction ≥ 20% de la somme du volume du neurofibrome plexiforme (NP) «cible» dans les 12 mois, confirmée par une IRM de suivi après ≥ 24 semaines

